深度解析人参植物源性细胞外囊泡在糖尿病创面愈合中的应用
糖尿病创面愈合障碍是糖尿病最棘手的并发症之一,其病理核心在于高糖微环境下血管生成障碍与免疫炎症失衡的恶性循环。糖尿病创面之所以长期难愈,并不只是因为“伤口大”或“感染重”,而是因为高糖环境会同时打乱氧化还原平衡、血管生成、炎症消退和细胞迁移等多个修复环节。慢性创面的核心病理特征,往往表现为局部ROS积累、内皮功能受损、巨噬细胞炎症表型持续活化以及再上皮化迟缓,这使得单一靶点的治疗方式很难真正改变局部微环境。也正因为如此,具备多成分、多靶点、低免疫原性特征的天然纳米递送系统,逐渐成为创面修复研究中的重要方向。
在这一背景下,人参不再只是传统意义上的“补气中药”,而是被重新定义为一种可供开发的天然生物材料来源。近年来围绕人参来源细胞外囊泡、人参来源囊泡纳米颗粒和外泌体样纳米颗粒的研究表明,这类颗粒既保留了植物来源材料易获取、成本相对可控、天然相容性较好的优势,又能携带脂质、核酸和次生代谢物等多类货物,形成比单一活性成分更复杂的生物学效应。这使得人参植物源性细胞外囊泡逐渐从“概念性发现”走向“应用型证据积累”。
一、从人参到囊泡:材料本身已经具备研究价值
人参来源细胞外囊泡研究最重要的第一步,是证明这类颗粒能够被稳定分离并完成标准化表征。2022年关于利用蔗糖梯度离心法分离和表征人参来源外泌体样纳米颗粒(GDEs)的一项研究显示,通过68%与27%蔗糖缓冲配合超速离心,可以从人参中获得较为均一的外泌体样纳米颗粒[2]。

(图1)人参来源外泌体样纳米颗粒(GDEs)的分离。a. 取四年生人参,放入含有1×磷酸盐缓冲液(PBS)的搅拌机中。b. 将人参汁依次低速离心,以去除碎片。c. 将68%和27%的蔗糖垫层溶液缓慢加入超速离心用的聚碳酸酯离心管中,避免两层混合,然后将上清液轻轻转移至离心管内。超速离心后,收集蔗糖垫层之间的纳米囊泡。d. 为分离GDEs,采用蔗糖梯度(8/30/45/60%)对纳米囊泡进行纯化。在8%与30%蔗糖层之间获得GDEs。
其平均粒径约为105.8 nm,表面电位约为−20.7 mV,NTA测得浓度约为2.05×1013 particles/mL。此外,冻干后的颗粒在室温下可保持稳定长达60天。这一结果的意义在于,它把“人参有效成分”从传统浸提物的混合概念,推进到了“可定义、可测量、可追踪的纳米颗粒”层面[2]。

(图2)人参来源外泌体样纳米颗粒(GDEs)的表征。a. GDEs的分离。b. 纳米颗粒追踪分析结果,显示GDEs的粒径分布和颗粒数。c. GDEs的透射电子显微镜图像。d. 动态光散射分析结果,显示GDEs的粒径和zeta电位。
2024年发表于《Journal of Ginseng Research》的一项关于人参来源外泌体样纳米颗粒保护皮肤免受紫外线照射和氧化应激损害的研究,进一步地把材料学证据补得更完整。研究者从人参来源的外泌体样纳米颗粒中鉴定出了多种人参皂苷成分,包括Re、Rg1、Rb1、Rf、Rg2(S)、Gyp17、Rd、C-Mc1、C-O和F2,说明这类囊泡并不是空载体,而是确实负载了与人参药效相关的活性分子[3]。

(表1)人参来源外泌体样纳米颗粒中的人参皂苷含量。GrDENs,人参来源外泌体样纳米颗粒;SD,标准差;ND,未检测到。
这一点非常关键,因为糖尿病创面修复并不需要单一“强效分子”,而更需要能够同时干预氧化应激、炎症反应和细胞修复程序的复合型材料。人参来源细胞外囊泡的货物复杂性,恰好与这种需求相吻合。
二、人体相关细胞证据:先证实它能影响皮肤细胞
人参来源细胞外囊泡真正进入生物医学应用讨论,是从人体皮肤细胞研究开始的。2021年一项关于人参来源细胞外囊泡促进人类皮肤细胞的抗衰老作用的研究以人真皮成纤维细胞和人表皮黑色素细胞为对象,证明了来自人参和人参细胞培养上清的细胞外囊泡能够改善复制性衰老或紫外线诱导的衰老相关表型,并降低与衰老、黑色素生成相关的分子表达[1]。这项工作虽然并非直接以创面为对象,但它提示了一个非常重要的前提:人参来源细胞外囊泡能够作用于人体皮肤细胞,并改变与修复能力密切相关的基础生物学状态。
2024年,研究人员在人参来源外泌体样纳米颗粒保护皮肤免受紫外线照射和氧化应激的损害的研究中进一步证明,人参来源外泌体样纳米颗粒对皮肤损伤的保护并不局限于“抗老”,而是延伸到了抗氧化应激和抗紫外损伤[3]。研究显示,这类颗粒可在UV 或H₂O₂刺激条件下减少ROS生成,降低细胞死亡,并抑制AP-1相关信号和一系列与凋亡、衰老、炎症有关的分子变化[3]。

(图3)人参来源外泌体样纳米颗粒(GrDENs)处理HaCaT细胞后的细胞活力和细胞内ROS水平。 (A和B) A图中,HaCaT细胞单独用GrDENs(0–2×10⁹个颗粒/mL)处理24小时。B图中,HaCaT细胞预先用GrDENs(0–2×10⁹个颗粒/mL)处理30分钟,然后用UVB照射24小时。采用MTT法检测细胞活力。 (C和D)HaCaT细胞预先用GrDENs(0–2×10⁹个颗粒/mL)处理30小时,然后用UVB照射24小时,之后分别用H2DCFDA (C)或DCFH-DA (D)孵育20分钟。采用荧光成像(C)和流式细胞术(D)测定细胞内ROS水平。荧光强度用ImageJ软件测量(C)。图(A)、(B)和(C)中的数据以至少三次独立实验的平均值±标准差表示。图(D)中的结果为三次独立实验的代表性图像。##p < 0.01 与正常组(未处理)相比,*p < 0.05,**p < 0.01 与对照组(紫外线照射)相比。
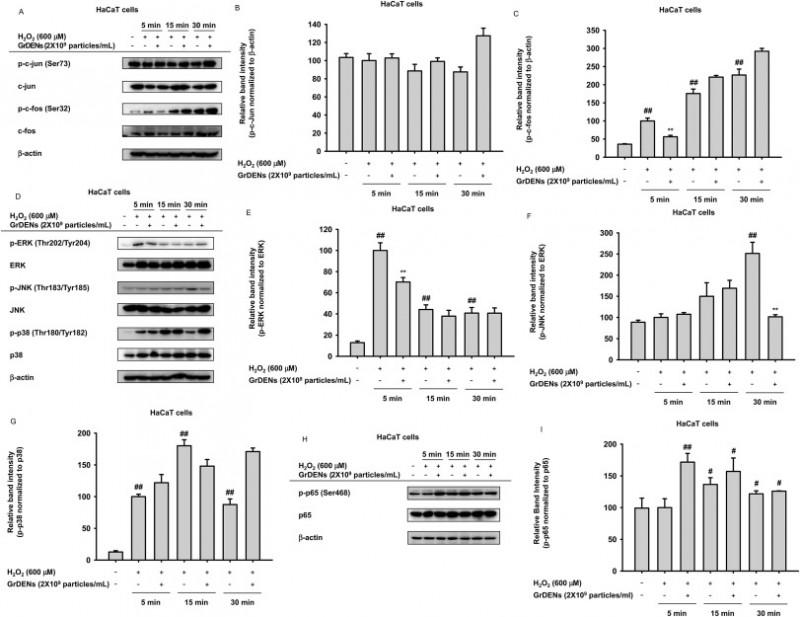
(图4)人参来源外泌体样纳米颗粒(GrDENs)对AP-1信号通路的影响。HaCaT细胞预先用GrDENs(2×10⁹个颗粒/mL)处理30分钟,然后用H₂O₂处理,处理时间如图所示。(A-C)通过免疫印迹法检测AP-1亚基的磷光水平和总蛋白水平,包括c-jun(A和B)和c-fos(A和C)。(D-G) 通过免疫印迹分析检测AP-1通路相关分子(如ERK(D和E)、JNK(D和F)和p38(D和G))的磷光水平和总蛋白水平。(H和I)通过免疫印迹分析检测NF-κB通路相关分子p65的磷光水平和总蛋白水平。使用ImageJ软件测量条带强度,并将磷酸化蛋白的相对条带强度标准化至相应的总蛋白水平。图(B)、(C)、(E)、(F)、(G)和(I)中的数据以三次独立实验的平均值±标准差表示,代表性图像见图(A)、(D)和(H)。##p < 0.01,#p < 0.05与正常组(未处理组)相比,*p < 0.05,**p < 0.01与对照组(H₂O₂暴露组)相比。
这些结果说明,人参来源细胞外囊泡并不是简单地让细胞更活跃,而是在应激条件下帮助皮肤细胞恢复稳态,这恰好是慢性创面治疗最需要的生物学基础。
三、机制层面:它为什么可能改善糖尿病创面
如果只看“能否促进愈合”,很多材料都可能在动物实验里给出积极结果;真正决定其转化价值的,是能不能解释清楚机制。人参来源纳米颗粒(GDNPs)的优势,在于其已经被证明能够同时影响增殖、迁移、血管生成和炎症控制等多个环节。2023年一项关于人参来源纳米颗粒可促进皮肤细胞增殖并促进伤口愈合的研究表明,GDNPs可促进皮肤细胞增殖并加快小鼠创面愈合,其作用与ERK以及AKT/mTOR信号通路激活有关[5]。这意味着它并不是单纯抑制损伤,而是推动创面进入再生程序。

(图5)GDNPs通过ERK和AKT/mTOR通路调控HaCaT细胞增殖。将HaCaT细胞与不同浓度的GDNPs孵育48小时。采用Western blotting法检测细胞周期蛋白D1、细胞周期蛋白B1、p-AKT、AKT、p-ERK、ERK、p-mTOR、mTOR、P70S6K(S6K)、p-S6K、eIF4G和微管蛋白的蛋白表达水平。检测微管蛋白是为了确认胞质组分中各蛋白的含量相等。所示结果为三个独立实验的代表性结果,三个独立实验的结果相似(*p<0.05,**p<0.01,***p<0.001,与对照组相比)。
2025年,长春中医药大学赵大庆教授研究团队在Materials Today Bio上发表了题为“Ginseng-derived nanoparticles accelerate diabetic wound healing by modulating macrophage polarization and restoring endothelial cell function”的文章,则把这一逻辑进一步推进到糖尿病创面的病理微环境中。该研究显示,GDNPs可缓解高糖联合H₂O₂诱导的内皮细胞损伤,恢复其愈合与成血管能力。转录组、富集分析及蛋白印迹证实,GDNPs可通过激活PI3K/AKT/HIF-1α通路增强血管生成,该效应可被LY294002或AKT siRNA阻断,进而揭示GDNPs通过该信号轴促进血管生成的分子机制[4]。
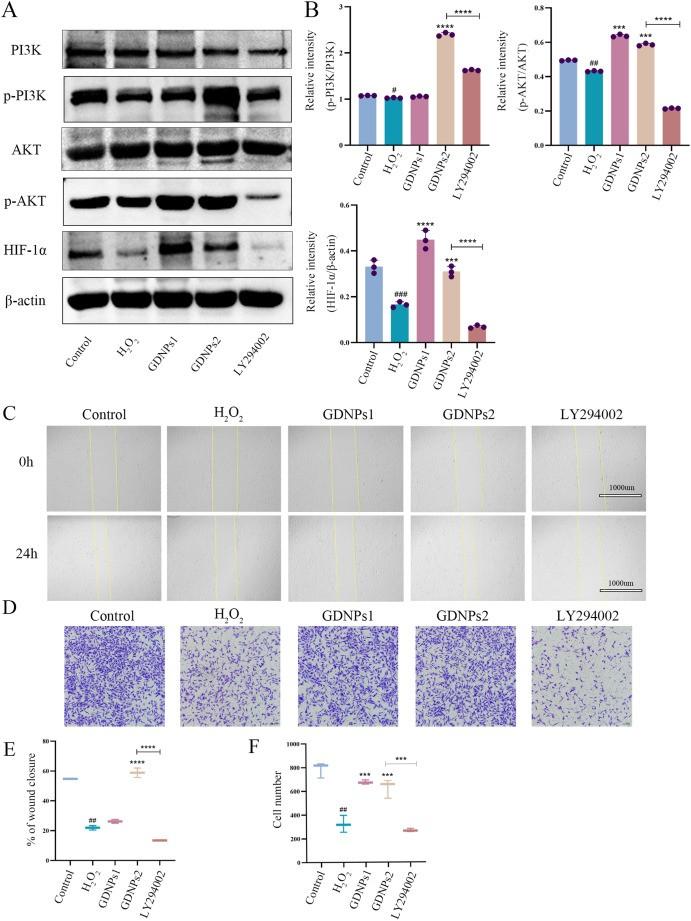
(图6)人参来源纳米颗粒(GDNPs)通过激活PI3K/AKT/HIF-1α信号通路促进血管生成。HUVECs中PI3K、p-PI3K、AKT、p-AKT和HIF-1α的免疫印迹分析(A)。p-PI3K/PI3K、p-AKT/AKT和HIF-1α/β-actin蛋白水平的定量分析(B)。Western blot结果以β-actin进行标准化。使用PI3K抑制剂LY294002进行HUVECs划痕愈合实验(C)。Transwell评估HUVECs的细胞迁移能力(D)。划痕愈合率的定量分析(E)。迁移细胞数量的定量分析(F)。(n = 3个独立实验)。Control:对照组;H₂O₂:H₂O₂模型组;GDNPs1:H₂O₂+GDNPs(10 μg/ml);GDNPs2:H₂O₂+GDNPs(20 μg/ml);LY294002:H₂O₂+GDNPs2(20 μg/ml)+LY294002 (10 μM),##p < 0.01与对照组相比,***p < 0.001与H₂O₂组相比。

(图7)人参来源纳米颗粒(GDNPs)通过激活PI3K/AKT/HIF-1α信号通路促进血管生成。HUVECs中AKT、p-AKT和HIF-1α的免疫印迹分析(A)。AKT/β-actin、p-AKT/AKT和HIF-1α/β-actin蛋白水平的定量分析(B)。Western blot结果以β-actin进行标准化。使用AKT siRNA进行HUVECs划痕愈合实验(C)。Transwell评估HUVECs的细胞迁移能力(D)。划痕愈合率的定量分析(E)。迁移细胞数量的定量分析(F)。(n = 3个独立实验)。Control:对照组;H₂O₂:H₂O₂模型组;GDNPs:H₂O₂+GDNPs(20 μg / ml)。siControl:H₂O₂+GDNPs(20 μg/ml)+阴性对照siRNA(50 nM);siAKT:H₂O₂+GDNPs(20 μg/ml)+AKT siRNA(50 nM)。
同时,免疫荧光、流式及蛋白印迹证实,GDNPs能诱导巨噬细胞由M1向M2极化。转录组学显示其抑制TLR4/MyD88/MAPK通路过度激活并减少炎症介质NO生成,经TAK-242与SP600125验证该通路关键作用,阐明GDNPs通过调控此信号轴促进M2极化及抗炎的分子机制[4]。

(图8)人参来源纳米颗粒(GDNPs)通过抑制TLR4/MyD88/MAPK通路的激活,促进巨噬细胞M2极化并减弱炎症反应。RAW264.7细胞中TLR4、MyD88、JNK、p-JNK、P38、p-P38、ERK和p-ERK的免疫印迹分析(A)。定量分析TLR4/β-actin、MyD88/β-actin、p-JNK/JNK、p-P38/P38和p-ERK/ERK的蛋白水平(B)。Western blot结果以β-actin进行标准化。RAW264.7细胞中NO的水平(C)。Control:对照组;H₂O₂:H₂O₂模型组;GDNPs1:H₂O₂+GDNPs (10 μg/ml)。GDNPs2:H₂O₂+GDNPs (20 μg/ml);GDNPs3:H₂O₂+GDNPs (40 μg/ml),#p < 0.05,##p < 0.01与对照组相比,∗p < 0.05,∗∗p < 0.01,∗∗∗p < 0.001与 H₂O₂组相比。
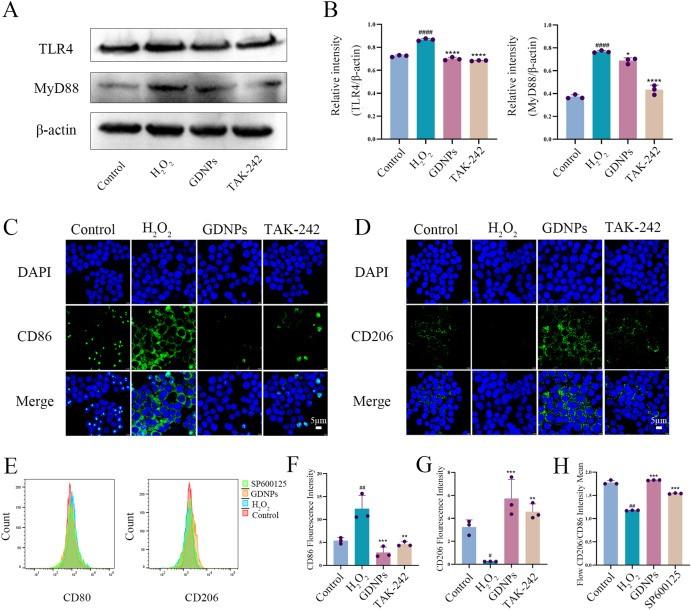
(图9)人参来源纳米颗粒(GDNPs)通过抑制TLR4/MyD88/MAPK通路激活,促进巨噬细胞M2极化并减弱炎症反应。RAW264.7细胞中TLR4、MyD88和β-actin的免疫印迹分析(A)。TLR4/β-actin和MyD88/β-actin蛋白水平的定量分析(B)。Western blot结果以β-actin进行标准化。RAW264.7细胞中CD86的免疫荧光检测(C)。RAW264.7细胞中CD206的免疫荧光检测(D)。RAW264.7细胞中CD206/CD80定量流式细胞术分析(E)。RAW264.7细胞中CD86荧光强度的定量图(F)。RAW264.7细胞中CD206荧光强度的定量图(G)。CD206/CD80的定量图(H)。(n = 3个独立实验) 。对照:对照组;H₂O₂:H₂O₂模型组;GDNPs:H₂O₂+GDNPs(20 μg / ml);TAK-242:H₂O₂+TAK-242(100 nM)。SP600125:H₂O₂+SP600125(10 μM),# p < 0.05,## p < 0.01,### p < 0.001与对照组相比,∗p < 0.05,∗∗p < 0.01,∗∗∗p < 0.001与H₂O₂组相比。
这一机制设计的价值在于,它并未将创面修复简化为单纯“长新肉”,而是同时处理了“血供重建不足”和“炎症拖延不退”这两个核心障碍。对糖尿病慢性创面而言,这种“双向重塑”比单一促生长更接近真实临床需求。
从整体上看,这些研究共同构成了一条较为清晰的逻辑链:人参来源细胞外囊泡可以被稳定分离,能够承载多种活性货物,可以进入皮肤相关细胞并改善其应激状态,还能在动物创面模型中通过促进血管生成、抗氧化和抑制炎症来改善愈合进程。这条链条说明,人参植物源性细胞外囊泡已经不是“有没有可能有效”的问题,而是“如何进一步标准化、工程化和验证其临床适用性”的问题。
四、从科研到转化:植物囊泡的价值不止于一个模型
对慢性创面来说,真正有前景的不是某个单一分子,而是能够在复杂微环境中同时处理多重病理障碍的系统性方案。人参植物源性细胞外囊泡的研究价值,正在于它提供了这样一种可能:以天然来源的纳米颗粒为载体,以多货物协同为基础,以抗炎、抗氧化、促血管生成和促再上皮化为核心输出,去重建糖尿病创面的修复平衡。从应用开发角度看,这种材料很适合继续向制剂化、贴敷化和局部递送方向推进。
北京泓九生命科学研究院的技术研发团队从这一方向切入,重点并不在于重复已有动物实验,而在于把植物源性细胞外囊泡的制备、负载、递送和验证流程进一步工程化。研究院创立的专属品牌UICN(Ultra-Intelligent Cargo Nanovesicles)承载了这类技术叙事,强调的是“智能装载”和“定向递送”,而不是单纯的概念包装。把人参植物源性细胞外囊泡放进UICN这一品牌体系中,最有价值的表达应当是它如何成为一个更标准化、更可控的天然纳米载体平台,而不是停留在“传统植物提取物升级版”的层面。
结语
总体而言,人参植物源性细胞外囊泡的研究,已经从基础材料分离,逐步走到了人体相关细胞验证、机制解析和糖尿病创面动物模型验证的阶段。对慢性创面修复而言,它提供的不只是一个新的植物来源材料,更是一种新的修复思路:借助天然囊泡重建局部微环境,让创面修复从“被动等待闭合”转向“主动推动再生”。这正是人参样囊泡纳米颗粒最值得继续深挖的地方。
参考文献
[1] Cho E-G, Choi S-Y, Kim H, Choi E-J, Lee E-J, Park P-J, Ko J, Kim K-P, Baek H-S. Panax ginseng-Derived Extracellular Vesicles Facilitate Anti-Senescence Effects in Human Skin Cells. Cells. 2021;10(3):486. doi:10.3390/cells10030486. PMID:33668388.
[2] Kim J, Lee Y-H, Wang J, Kim YK, Kwon IK. Isolation and characterization of ginseng-derived exosome-like nanoparticles with sucrose cushioning followed by ultracentrifugation. SN Applied Sciences. 2022;4:63. doi:10.1007/s42452-022-04943-y.
[3] Choi W, Cho JH, Park SH, Kim DS, Lee HP, Kim D, Kim HS, Kim JH, Cho JY. Ginseng root-derived exosome-like nanoparticles protect skin from UV irradiation and oxidative stress by suppressing activator protein-1 signaling and limiting the generation of reactive oxygen species. Journal of Ginseng Research. 2024;48(2):211-219. doi:10.1016/j.jgr.2024.01.001.
[4] Fan L, Jia X, Dong F, Yang S, Li W, Zhao R, Yin L, Zhao D, Wang J. Ginseng-derived nanoparticles accelerate diabetic wound healing by modulating macrophage polarization and restoring endothelial cell function. Materials Today Bio. 2025;34:102143. doi:10.1016/j.mtbio.2025.102143.
[5] Yang S, Lu S, Ren L, Bian S, Zhao D, Liu M, Wang J. Ginseng-derived nanoparticles induce skin cell proliferation and promote wound healing. Journal of Ginseng Research. 2023;47(1):133-143. doi:10.1016/j.jgr.2022.07.005.
(来源:科技信息网)


